Εκδόσεις ΜΠΑΧΑΡΑΚΗ – Χημεία Θετικής Κατεύθυνσης
46
Υδατικό διάλυμα Δ
1
περιέχει ασθενές οξύ ΗΑ. 50mL του διαλύματος Δ
1
ογκομετρούνται με πρότυπο διάλυμα Δ
2
ΝaΟΗ συγκέντρωσης 0,2Μ. Στο
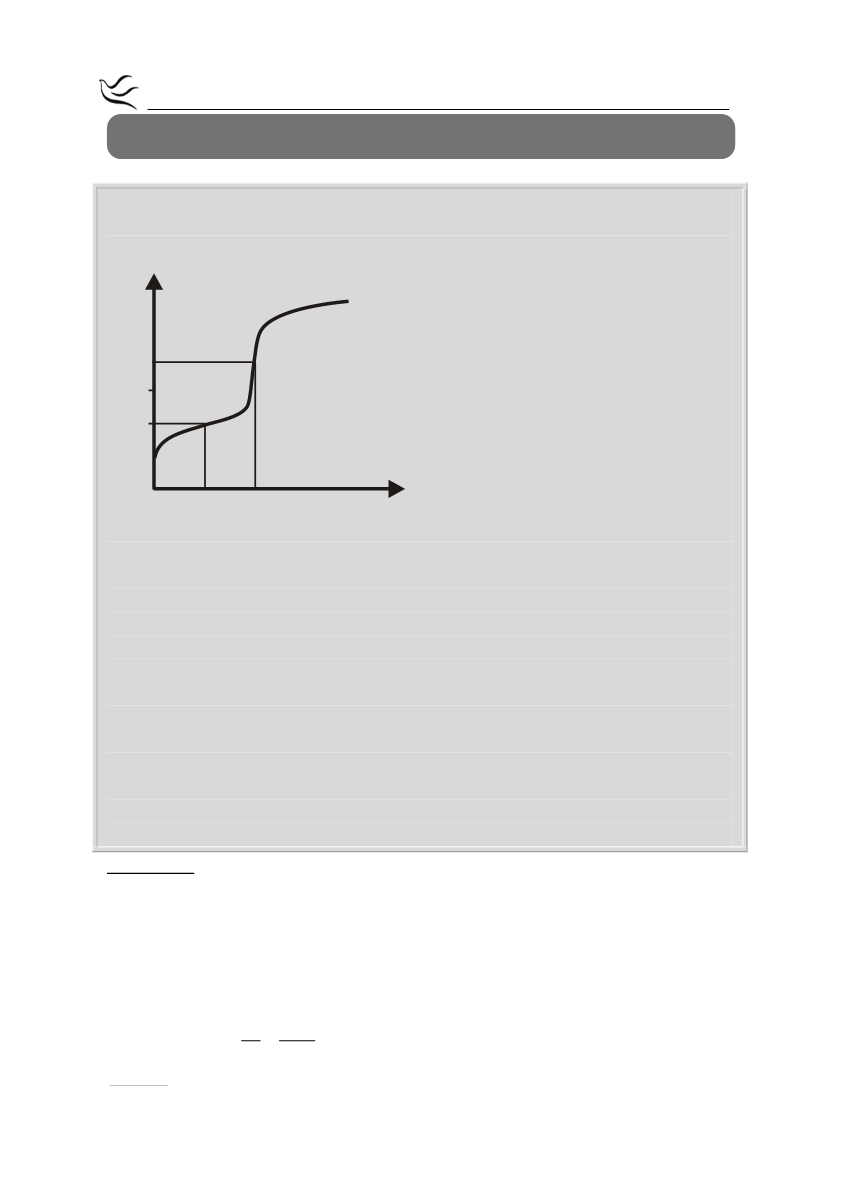
παρακάτω σχήμα δίνεται η καμπύλη της ογκομέτρησης:
Για την πλήρη εξουδετέρωση του ΗΑ απαιτούνται 50mL του διαλύματος Δ
2
.
4.1.
Να υπολογίσετε τη συγκέντρωση του οξέος ΗΑ στο διάλυμα Δ
1
.
(Μονάδες 4)
4.2. α.
Στο σημείο Β της καμπύλης ογκομέτρησης έχουν προστεθεί 25mL του
προτύπου διαλύματος Δ
2
και το pΗ του διαλύματος που προκύπτει είναι 5. Να
υπολογίσετε τη σταθερά ιοντισμού Κ
a
του οξέος ΗΑ.
β.
Να υπολογίσετε το pΗ του διαλύματος στο ισοδύναμο σημείο.
(Μονάδες 8+7=15)
4.3.
Υδατικό διάλυμα Δ
3
ασθενούς οξέος ΗΒ 0,1Μ έχει pΗ=2,5. Ποιο από τα
δύο οξέα ΗΑ, ΗΒ είναι το ισχυρότερο;
(Μονάδες 6)
Δίνονται:
Όλα τα διαλύματα βρίσκονται σε θερμοκρασία θ=25°C, όπου Κ
w
= 10
-14
.
Τα αριθμητικά δεδομένα του προβλήματος επιτρέπουν τις γνωστές
προσεγγίσεις.
Απάντηση:
4.1.
Υπολογίζουμε τα mol του ΝαΟΗ στα 50ml του Δ
2
:
2 2 2
n C V 0,2 0,05 0,01mol
2
1mol
1mol
x; 0,01mol
HA NaOH NaA H O
ά x 0,
ρα
01mol
1
HA
1
n 0,01
C
0,2M
V 0,05
pH
7
5
A
B
25 50
(Ισοδύναμο Σημείο)
ΘΕMA 4o
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ 2006









